TỔNG QUAN VỀ HYDRGEL
1. Khái niệm về hydrogel
Năm 1955, Giáo sư Lim và Wichterle, Prague, Cộng hòa Czech đã điều chế ra hydrogel đầu tiên với tiềm năng ứng dụng trong lĩnh vực y sinh [1]. Cho đến nay, hydrogel đã được ứng dụng trong nhiều lĩnh vực.
Hydrogel là các polymer được liên kết với nhau, bản chất ưa nước của polymer dẫn tới hydrogel có thể hấp thụ một lượng nước lớn. Thành phần, cấu trúc của một hydrogel có thể được thiết kế cho ứng dụng chuyên biệt bằng cách lựa chọn các vật liệu ban đầu và quy trình kỹ thuật phù hợp [2, 3].
2. Phân loại hydrogel
Có nhiều cách để phân loại hydrogel như dựa vào nguồn gốc, dựa vào thành phần polymer, dựa trên loại liên kết ngang. Trong nghiên cứu này, hydrogel được phân loại theo cách thức hình thành các liên kết ngang bằng phương pháp vật lý hoặc phương pháp hóa học [4].
Có thể phân loại hydrogel theo những liên kết ngang hình thành gel hóa học (mối tương tác hóa học giữa các phân tử polymer) và gel vật lý (mối tương tác vật lý giữa các phân tử polymer). Những phương pháp tạo liên kết ngang khác nhau để tạo hydrogel được sử dụng để đạt được các đặc tính riêng biệt, như thời gian gel hóa, tính chất cơ lý, và tương hợp sinh học. Các tính chất này của hydrogel rất quan trọng cho các ứng dụng trong cấy ghép và tái tạo mô.
3. Tổng hợp hydrogel
Tổng hợp hydrogel là quá trình tạo liên kết ngang giữa các phân tử polymer trong môi trường nước bằng các phương pháp khác nhau như: polymer hóa gốc tự do, tạo liên kết ngang bằng phản ứng trên các nhóm chức của polymer, tạo liên kết ngang bằng phản ứng xúc tác enzyme, tạo liên kết ngang bằng phức lập thể, tạo liên kết ngang bằng tác dụng nhiệt, tạo liên kết ngang bằng cách tạo siêu phân tử, tạo liên kết ngang bằng phức cyclodextrin, tạo liên kết ngang bằng cách kết hợp tương tác vật lý và tương tác hóa học.
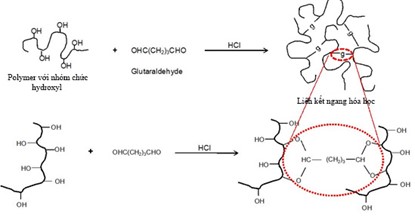
Hình 1. Liên kết ngang
- Tạo liên kết ngang bằng sự polymer hóa gốc tự do
Tổng hợp các hydrogel ứng dụng trong sinh học, người ta thường dùng polymer hóa gốc tự do [5]. Các chất dùng để tạo gốc tự do như chất khơi mào nhạy sáng, chất khơi mào oxi hóa khử…
Ưu điểm của chất khơi mào nhạy ánh sáng là tạo liên kết ngang nhanh, và bất lợi là khi tiếp xúc với UV ở cường độ cao hoặc thời gian dài có thể ảnh hưởng xấu đến hoạt động trao đổi chất của tế bào. Ngoài ra, nhiệt phát sinh trong quá trình tạo liên kết ngang có thể gây hoại tử tế bào. Vì vậy, cường độ của tia cực tím được giới hạn trong khoảng 5-10 mW/cm2 để ngăn sự hủy hoại tế bào.
Ngoài ra, các chất khơi mào oxi hóa khử như: N, N, N’, N’-tetramethyl ethylenediamine (TEMED) và amoni peroxydisulfate (APS) được dùng làm chất khơi mào trong hydrogel. Tăng nồng độ chất khơi mào sẽ giảm thời gian gel hóa và tăng cường tính cơ học. Tuy nhiên, nồng độ chất khơi mào cao (10 mM) sẽ gây độc tế bào cao dẫn tới tỉ lệ sống của tế bào thấp (nhỏ hơn 30%) sau 3 ngày nuôi cấy tế bào.
-Tạo liên kết ngang bằng phản ứng trên các nhóm chức của polymer.
Hydrogel có thể được tổng hợp thông qua các phản ứng giữa các nhóm chức như phản ứng Schiff-base, phản ứng cộng Michael.
Phản ứng Schiff-base giữa một nhóm aldehyde và một nhóm amine thường được sử dụng để điều chế các hydrogel liên kết ngang.
Phản ứng cộng Michael giữa một tác nhân thân hạch (một amine hoặc một nhóm thiol) và một tác nhân thân điện tử (vinyl/acrylate/nhóm maleimide) là một phương pháp khác để tạo hydrogel, đặc biệt là các hydrogel dùng để tiêm trong kỹ thuật mô. Hydrogel được tạo thành đơn giản bằng cách trộn hai polymer mang nhóm thân hạch và nhóm thân điện tử. Các hydrogel được tạo thành qua phản ứng cộng Michael có thời gian gel hóa trung bình từ 0,5 đến 60 phút. Thời gian gel có thể được điều chỉnh thông qua mật độ liên kết ngang. Do phản ứng cộng Michael diễn ra trong điều kiện êm dịu nên các phản ứng không ảnh hưởng nghiêm trọng đến sự tồn tại của tế bào trong suốt quá trình hình thành hydrogel. Thông thường, các tế bào được kết hợp trong hydrogel vẫn có thể tồn tại từ vài ngày đến vài tháng. Tuy nhiên, việc dùng dư các nhóm chức thiol vì thiol có thể gây chết tế bào [7-10].
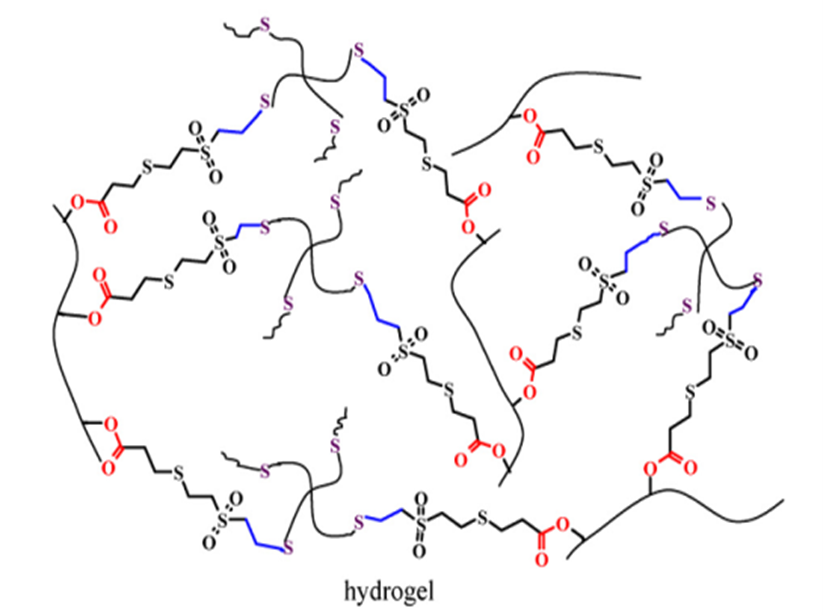
Hình 2. : Phản ứng Michael
- Tạo liên kết ngang bằng phản ứng xúc tác enzyme.
Enzyme thường cho thấy tính đặc hiệu cao, có khả năng tránh được phản ứng phụ trong quá trình tạo liên kết ngang. Điều này giúp kiểm soát và dự đoán các động học của sự gel hóa và làm tăng tỷ lệ liên kết ngang bằng cách điều chỉnh nồng độ enzyme. Các enzyme thường được sử dụng để tổng hợp hydrogel như: Transglutaminase, Tyrosinase, Horseradish peroxidase.
Transaminase có nhiều trong cơ thể người, enzyme này tham gia vào quá trình xúc tác cho phản ứng amide dẫn đến hình thành nối liên kết ngang N-C(g-glutamyl) lysine giữa 2 protein và dẫn đến hình thành hydrogel trên cơ sở các protein có độ tương hợp sinh học cao [11].
Enzyme Tyrosinase là enzyme phổ biến trong nấm rơm có thể oxi hóa các phenol có khối lượng phân tử thấp hoặc các phần tyrosine trong protein thành các quinone, sau đó những quinone này có thể phản ứng trực tiếp với các nhóm amine của các protein hoặc các hợp chất mang amine như chitosan tạo thành các hydrogel sinh học [13].
Horseradish peroxidase (HRP) là enzyme (hemoprotein) được sử dụng gần đây trong tổng hợp in situ nhiều loại hydrogel. Trong phản ứng tạo hydrogel, enzyme HRP xúc tác cho phản ứng ghép cặp của các hợp chất có phenol hoặc aniline trong sự hiện diện của lượng nhỏ chất oxi hóa H2O2. Cơ chế xúc tác hình thành gốc tự do phenoxyl của enzyme HRP có sự hiện diện của H2O2. Phản ứng tạo liên kết ngang carbon-carbon hình thành ở vị trí ortho của 2 phân tử phenol hoặc carbon-oxygen ở vị trí ortho của phenoxy và gốc tự do phenoxyl. Nhiều loại hydrogel sinh học trên cơ sở các polysaccharide, protein, polymer tổng hợp được biến tính nhóm phenoxy và sử dụng trong điều chế hydrogel xúc tác enzyme HRP [15-17].
Nhìn chung phương pháp điều chế hydrogel bằng enzyme có những ưu điểm sau:
+ Thời gian tạo gel ngắn.
+ Dễ điều khiển quá trình tạo gel.
+ Điều kiện phản ứng êm dịu (nhiệt độ cơ thể, môi trường trung tính).
+ Không gây ra các phản ứng độc hại với mô, tế bào.
- Tạo liên kết ngang bằng tác dụng nhiệt.
Sự gel hóa nhạy nhiệt được kích hoạt bởi tương tác kỵ nước khi thay đổi nhiệt độ. Hydrogel nhạy nhiệt như poly(ethylene oxid)-poly(propylene oxid)-poly(ethylene oxid) (PEO-PPO-PEO), tên thương mại là Pluronic và poly(N-isopropylacrylamide) (PNIPAAm) được sử dụng phổ biến nhất. Tuy nhiên, do không suy giảm và có khả năng gây độc tế bào nên các polymer này bị hạn chế ứng dụng vào kỹ thuật cấy mô. Ví dụ, ở nồng độ 10% (w/w), dung dịch F127 Pluronic làm giảm đáng kể khả năng di chuyển các tế bào HepG2. Khi được giữ trong hydrogel với nồng độ F127 từ 15-20% các tế bào sẽ chết hoàn toàn trong vòng 5 ngày [29,30].
Những hydrogel nhạy nhiệt có khả năng suy giảm sinh học, chẳng hạn như các copolymer dạng khối hoặc dạng ghép có chứa các gốc PEO ưa nước và các gốc kỵ nước PLA, khả năng gây độc thấp hơn. Hydrogel nhạy nhiệt suy giảm sinh học cũng có thể được điều chế từ các polyme tự nhiên, chẳng hạn như gelatin và agarose. Những polymer tự nhiên tan trong nước khác như polysaccharide, có thể được biến tính với một nhóm kỵ nước để tạo ra hydrogel vật lý [18-20].
-Tạo liên kết ngang bằng tương tác ion.
Tương tác ion đã được nghiên cứu rộng rãi để tạo liên kết ngang trong quá trình gel hóa. Một lợi thế của phương pháp này là sự suy giảm sinh học có thể xảy ra như sự phân ly ion trong ngoại bào, phá vỡ mạng lưới liên kết ngang.
Tương tác ion có thể xảy ra giữa một phân tử polymer và một phân tử nhỏ hoặc giữa hai phân tử polymer trái dấu để tạo thành một hydrogel. Một ví dụ về liên kết ngang giữa một phân tử polymer và một phân tử nhỏ: liên kết polypeptide elastin được hình thành thông qua tương tác tĩnh điện giữa dư lượng ion dương lysine và ion âm phosphor hữu cơ trong điều kiện sinh lý. Một ví dụ khác về tương tác ion giữa hai phân tử polymer trái dấu là chuỗi peptide với các ion âm và ion dương xen kẽ có thể tự lắp ráp để tạo thành hydrogel [21, 22].
Tương tác ion cũng có thể được sử dụng để tạo liên kết ngang hạt nano gel, nhằm tạo ra chuỗi phân tử ba chiều thích hợp cho mang nhả thuốc. Ví dụ, vi cầu dextran được hình thành do tương tác phức tạp giữa các vi hạt tích điện trái dấu.
-Tạo liên kết ngang bằng liên kết hydro
Hydrogel hình thành nhờ tương tác tạo liên kết hydro có thể được thực hiện bằng cách tăng hoặc giảm nhiệt độ đến nhiệt độ đông đặc. Poly(vinyl ancohol) là một hydrogel điển hình được tạo thành theo phương pháp này. Hỗn hợp của hai hay nhiều các polyme tự nhiên có thể có sự đồng bộ về tính lưu biến, có nghĩa là các tính đàn hồi, độ nhớt của hỗn hợp polymer giống gel nhiều hơn so với các tính chất này ở từng polymer riêng lẻ.
TÀI LIỆU THAM KHẢO
1. Iwona G. and Helena J., (2010), Review: Synthetic Polymer Hydrogels For Biomedical Applications, Chemistry & Chemical Technology, ( 4), 4, 297-304
2. Ahmed E.M, (2015), Hydrogel: Preparation, characterization and applications, Journal of Advanced Research, (2), 6, 105-121.
3. Sophie R., Gert S. and Wim E. (2008), In situ gelling hydrogels for pharmaceutical and biomedical applications, International Journal of Pharmaceutics, 355, 1–18.
4. Nilimanka D. (2013), Preparation Methods And Properties Of Hydrogel, International Journal Of Pharmacy And Pharmaceutical Sciences, (3) 5, 112-117.
5. Jason A., Robert L. (2011), Biomaterials for Tissue Engineering Applications, Springer Wien NewYork, 9-47.
6. Assaf S. (2011), Progress in Molecular and Environmental Bioengineering - From Analysis and Modeling to Technology Application, Hydrocolloids Research Centre Glyndwr University, Wrexham, United Kingdom, 117-151.
7. Pek S., Kurisawa M., Gao S., Chung J., Ying J. (2009), The development of a nanocrystalline apatite reinforced crosslinked hyaluronic axit–tyramin composit as an injectable bone cement, Biomaterials, 30, 822–828.
8. Chen JP, Tsai MJ, Liao HT, (2013), Incorporation of biphasic calcium phosphate microparticles in injectable thermoresponsive hydrogel modulates bone cell proliferation and differentiation, Colloids Surf B Biointerfaces, 110, 120-129.
9. Tianhong Chen, Heather D. Embree, Eleanor M. Brown, Maryann M. Taylor, Gregory F. Payne, (2003), Enzyme-catalyzed gel formation of gelatin and chitosan: potential for in situ applications, Biomaterials, 24, 2831–2841
10. Kobayashi, S., Uyama, H. & Kimura, S. (2001), Enzymatic Polymerization, Chem. Rev., (12) 101, 3793–3818.
11. Lee, F., Chung, J.E., Kurisawa, M. (2009), An Injectable Hyaluronic Axit-Tyramin Hydrogel System for Protein Deliver, Journal of Controlled Release, (3)134, 186-193.
12. Ngoc Quyen Tran, Yoon Ki Joung, Eugene Lih, K. Min Park, Ki Dong Park (2010), Supramolecular hydrogels exhibiting fast in situ gel forming and adjustable degradation properties; Biomacromol.,11: 617-625.
13. Ngọc Quyen Tran, Yoon Ki Joung, Eugene Lih, K. Min Park, Ki Dong Park (2011), RGD-Conjugated In Situ Forming Hydrogels as Cell-Adhesive Injectable Scaffolds, Macromolecular Research, 19, 300-306.
14. Tsuji H. (2005), Poly(lactide) stereocomplexes: Formation, structure, properties, degradation, and applications, Macromolecular Bioscience, (7) 5, 569-597.
15. Gert W. B., John J. L. J., Jan W. K., Sophie V. T., Theo V., Cornelus F. N., Willem D. O., Wim E. H. (2004), In situ crosslinked biodegradable hydrogels loaded with IL-2 are effective tools for local IL-2 therapy, European Journal of Pharmaceutical Sciences, (4) 21, 561-567.
16. Hoarea T.R. and D.S. Kohane (2008), Hydrogels in drug delivery: Progress and challenges, Polymer, (8) 49, 1997-2007.
17. Harada A., J. Li, and M. Kamachi (1994), Double-stranded inclusion complexes of cyclodextrin threaded on poly(ethylene glycol), Nature, 370, 126-128.
18. Xian J. L., Oren A. S. (2013), Polymeric and Self Assembled Hydrogels, The Royal Society of Chemistry, Cambridge, UK, 10-63.
19. Xiong, X.Y., K.C. Tam, and L.H. Gan (2006), Polymeric nanostructures for drug delivery applications based on pluronic copolymer systems, Nanoscience and Nanotechnology, 6, 2638-2650.
20. Omidian, H. and K. Park (2012), Fundamentals and applications of controlled release drug delivery, Springer, New York, 4, 75–106.
21. Gerald G, Karl-Friedrich A (2009), Hydrogel Sensors and Actuators, Springer: Boston, 65-82.
22. Junmin Zhu and Roger E Marchant (2011), Design properties of hydrogel tissue-engineering scaffolds, Expert Rev Med Devices, (5) 8, 607–626.
